Sperimentazioni genetiche e tabù infranti
Il 2020 è per la Cina e per il resto del mondo un anno di incertezza e di riconfigurazione delle priorità economiche e di sviluppo. La pandemia di Covid-19 ha messo in primo piano nuove necessità e obiettivi, drenando risorse da alcuni settori economici facendole convergere verso altri. Uno degli ambiti maggiormente interessati da questi rivolgimenti è senza dubbio quello delle biotecnologie. Se da una parte molti progetti di ricerca e sviluppo sono stati messi in standby, dall’altra, grazie a investimenti pubblici e privati, è stata potenziata la dotazione finanziaria a sostegno di alcuni ambiti specifici, in particolare quello dello sviluppo di terapie e vaccini in grado di tamponare la pandemia in corso.
Secondo Nature, nel maggio 2020 vi erano almeno 90 sperimentazioni di vaccini per il Covid-19. Tra le terapie al vaglio della comunità scientifica e delle case farmaceutiche vi sono quelle che scommettono sugli ultimi sviluppi dell’ingegneria genetica, come ad esempio la tecnica CRISPR,[1] di cui si tratterà ampiamente in questo contributo. La Cina si trova in prima linea in questi sforzi e non vi sono dubbi che negli anni avvenire consoliderà un ruolo di prim’ordine nella ricerca e nelle applicazioni dell’ingegneria genetica.
Ancor prima della pandemia di coronavirus, verso la fine del 2018, la Cina è entrata con veemenza al centro del dibattito globale in questo settore. Nel novembre di quell’anno, il professor He Jiankui della SUSTech annunciò al mondo, tramite un video caricato sulla piattaforma YouTube, di aver usato la tecnologia CRISPR-Cas9[2] sulla linea germinale umana,[3] modificando embrioni impiantabili con lo scopo di indurre una resistenza genetica all’HIV. Secondo quanto riportato dallo stesso He, le due gemelle nate dall’esperimento, Lulu e Nana, sono nate in buona salute (mentre un terzo neonato è venuto alla luce nel 2019). Del destino e delle condizioni dei tre bambini non si hanno aggiornamenti da allora.[4]
Com’era prevedibile, la disapprovazione della comunità scientifica fu chiara e unanime.[5] Con sorpresa di alcuni osservatori, tuttavia, non tardò a manifestarsi anche la condanna da parte del governo cinese, della comunità scientifica nazionale e della stessa università del professor He. Accusato di aver violato le norme nazionali e i principi etici che regolano gli esperimenti genetici e la procreazione assistita, di praticare medicina senza le dovute qualifiche, e di aver condotto tali esperimenti per accrescere il proprio prestigio, He Jiankui è stato condannato a scontare tre anni di reclusione e a pagare una sanzione di tre milioni di yuan (circa 360.000 Euro). La Commissione nazionale per la salute (NHC, secondo l’acronimo inglese) ha, inoltre, interdetto a vita i tre ricercatori da qualsiasi attività legata alla procreazione umana assistita.
Lo scandalo legato all’esperimento di He non è stato il primo indicatore di una potenziale faglia etica tra Cina e Occidente nell’ambito delle biotecnologie, in particolare nell’ingegneria genetica. All’inizio del 2015, il primo grande tabù relativo alla manipolazione genetica di embrioni umani fu infranto dal team di Huang Junjiu della Sun Yat-sen University. Il gruppo di ricerca inviò alla rivista Nature i risultati di un esperimento dove si affermava di aver manipolato embrioni umani non impiantabili usando CRISPR. Obiettivo dello studio era di correggere una mutazione responsabile della beta talassemia (conosciuta anche come anemia mediterranea). Le riviste Nature e Science rifiutarono la pubblicazione dell’articolo per motivi etici. La ricerca trovò rapidamente un’altra collocazione, la rivista Protein & Cell, una pubblicazione open access finanziata da enti collegati a vario titolo con il Ministero dell’istruzione cinese.[6]
Nonostante il dibattito apertosi nella comunità scientifica internazionale, il paper del team di Huang ricevette un’accoglienza positiva in Cina, in particolare nei social media e nella stampa nazionale. La stessa rivista Nature inserì Huang nella classifica dei migliori 10 scienziati del 2015. Il risultato della ricerca evidenziava che i margini di errore nell’utilizzo di CRISPR erano ancora troppo alti per poter applicare la tecnica sugli embrioni in maniera sicura. Infrangendo ancora un altro tabù, nel 2017, ricercatori della Guangzhou Medical University testarono CRISPR su embrioni impiantabili sperando di ottenere risultati migliori dello studio precedente. Anche in questo caso le reazioni della comunità scientifica furono di allerta e sospetto. Nonostante questo, altri esperimenti della stessa natura furono presto realizzati negli Stati Uniti, nel Regno Unito e in Svezia.
CRISPR-Cas9 e la corsa cinese al gene editing
Per capire perché CRISPR rappresenti un potenziale cambio di paradigma nelle biotecnologie è utile delinearne sinteticamente il funzionamento. CRISPR-Cas9, usando la nomenclatura più appropriata, è una modalità di editing genetico utilizzata per tagliare e modificare il DNA di un organismo con l’obiettivo di disabilitare o alterare specifiche funzioni genetiche. Tale processo è basato sulla naturale capacità di alcune tipologie di batteri di riconoscere e legarsi a un segmento preciso di genoma (grazie a una sequenza RNA che può essere riprogrammata in laboratorio) e recidere il DNA nella posizione target usando l’enzima Cas9, o altri enzimi simili, che agiscono come delle forbici molecolari. Il segmento rimosso, se necessario, può essere sostituito con una sequenza personalizzata di DNA.[7] L’aspetto rivoluzionario non risiede nella scoperta delle sequenze CRISPR nei batteri, già descritte con precisione alla fine degli anni Ottanta, bensì nelle applicazioni di ingegneria genetica messe a punto negli ultimi anni grazie alle proprietà di “forbice” dell’enzima Cas9.
Il primo brevetto per l’utilizzo di CRISPR-Cas9 venne depositato da Jennifer Doudna ed Emmanuelle Charpentier nel 2012. La tecnica proposta dalle due ricercatrici aumenta significativamente l’accuratezza dell’intervento sul genoma umano, animale e vegetale, semplificandone il processo e abbattendone i costi rispetto ad altre tecniche precedentemente utilizzate. Per questo motivo CRISPR è definito da alcuni specialisti come una tecnologia ready-to-use: grande accessibilità, costi bassi e semplicità di utilizzo. È dunque facile rendersi conto di quali possano essere gli interessi in gioco. Le applicazioni sono innumerevoli, dalla creazione di varietà di riso e grano resistenti a funghi e parassiti, a varietà di maiali e bovini più adatti all’industria alimentare, alle sperimentazioni sugli animali per testare farmaci e modelli di cura per l’uomo, fino agli interventi diretti sul genoma umano per combattere gravi malattie genetiche.
CRISPR è sicuramente una tecnologia promettente ed è quasi certo che rappresenterà il futuro della biotecnologia. La portata di questa tecnica è rilevante tanto quanto il machine learning lo è per il futuro del settore IT. Pechino ne è consapevole e, infatti, non ha perso tempo. Il Capitolo 23, sezione 4, del 13° Programma Quinquennale dispone di “procedere rapidamente nel facilitare le vaste applicazioni della genomica e di altre biotecnologie” e promuovere “lo sviluppo su larga scala di cure mediche personalizzate, nuovi farmaci, bio-breeding, e altri prodotti e servizi biotecnologici di nuova generazione”. I ricercatori cinesi sono stati i primi a sperimentare CRISPR sui primati nel 2014. Da allora, la corsa cinese è stata inarrestabile. Nella sperimentazione umana a scopo clinico, la Cina sembra presentarsi già come leader a livello internazionale, almeno per il numero di studi clinici condotti. Secondo il registro pubblico americano ClinicalTrials.gov,[8] vi sono attualmente 32 trial CRISPR registrati, di cui 15 portati avanti nella Greater China contro i 14 degli Stati Uniti (Figura 2). Università cinesi, istituti nazionali di ricerca, ospedali universitari, imprese consolidate e startup sono già impegnati a sperimentare CRISPR su molteplici versanti avvalendosi di una quantità ingente di fondi pubblici e privati.
Parallelamente a quanto accaduto per l’intelligenza artificiale, la Cina ha velocemente raggiunto gli Stati Uniti nelle pubblicazioni su CRISPR, nonostante il numero ancora basso di citazioni. Anche nei brevetti, la Cina sta adottando una strategia piuttosto aggressiva, da alcuni additata come prassi protezionistica per scoraggiare l’ingresso di imprese straniere nel mercato interno: la maggioranza dei brevetti in biotecnologie cinesi è, infatti, registrato unicamente a livello nazionale. La Cina è oggi al secondo posto nel numero di famiglie di brevetti CRISPR registrati dopo gli Stati Uniti, ma al primo posto nelle applicazioni industriali, agricole e zootecniche.[9]
Le controversie legate agli esperimenti sugli embrioni rischiano di oscurare la velocità con cui la Cina sta sperimentando CRISPR in tanti altri settori strategici. Nel campo della sperimentazione umana a scopo clinico e non riproduttivo, Deng Hongkui, immunologo della Peking University, è stato nominato tra i “10 scienziati più importanti del 2019” da Nature. Utilizzando cellule prelevate dal midollo umano e modificate con CRISPR, il gruppo di ricerca di Deng ha testato una nuova terapia per HIV e leucemia, ottenendo un successo significativo nella cura di quest’ultima.[10]
Nel campo delle biotecnologie vegetali, ricercatori come Li Jiayang e Gao Caixia dell’Institute of Genetics and Developmental Biology (IGDB) della Chinese Academy of Sciences sono all’opera per produrre varietà di grano, riso e altre piante da raccolto considerate essenziali per la sicurezza alimentare del paese. Utilizzando CRISPR, numerosi gruppi di ricerca stanno cercando di inibire i patogeni responsabili di infezioni, funghi e attacchi virali nelle piante.[11] La Syngenta, azienda leader nelle tecnologie agroindustriali, acquistata nel 2017 da ChemChina, sta impiegando CRISPR per potenziare varietà di soia, grano, mais, riso, pomodori e girasoli. Nella zootecnia, istituti e aziende cinesi stanno portando avanti con grande rapidità la sperimentazione di CRISPR su bovini, suini, primati, conigli, pollame e altri animali. Lo scopo è duplice: da una parte garantire un approvvigionamento alimentare sicuro e mitigare gli effetti economici e sociali disastrosi di eventi quali la peste suina africana del 2019, che ha messo in ginocchio un’intera filiera alimentare (per far fronte all’epidemia, il valore delle importazioni di suino in Cina è aumentato del 150% in un anno).[12] Dall’altra, l’utilizzo di CRISPR potrebbe rivelarsi cruciale per favorire lo sviluppo di organi animali trapiantabili nell’uomo.
Infine, come tutte le tecniche di tale portata, grande attenzione è posta sullo sviluppo della tecnologia abilitante. La Cina, coerentemente con il suo obiettivo di autosufficienza tecnologica, sta sviluppando strumentazioni autoctone per avanzare nell’ingegneria genetica. Per lavorare sul genoma occorrono costosissimi sequenziatori genetici, una categoria di dispositivi in cui l’Occidente è stato fino a pochi anni fa egemone assoluto. Tra le imprese cinesi attive nel campo del sequenziamento genomico, svetta tra tutte il Beijing Genomics Institute, nato nel 1999 come istituto di ricerca no-profit. Trasformatosi in seguito in un gruppo privato, BGI Genomics è cresciuto in poco tempo fino a diventare una delle più importanti aziende di sequenziamento del genoma vegetale, animale e umano, erodendo significative fette di mercato ai competitor occidentali. L’azienda MGI Tech, acquistata da BGI Group, è oggi produttrice di alcuni tra i sequenziatori più potenti e veloci sul mercato, divenendo una credibile competitor di Illumina, società californiana considerata lo stato dell’arte del sequenziamento a livello globale. I clienti della BGI Group sono oggi università, case farmaceutiche e laboratori di tutto il mondo. Secondo molti media report, l’azienda di Shenzhen avrebbe sequenziato più genomi umani di qualsiasi altra società, assicurandosi economie di scala tali da abbattere drasticamente il costo del sequenziamento. Nel 2019, BGI offriva un sequenziamento umano a partire da 600 dollari (da 100 milioni di dollari all’inizio degli anni 2000)[13] espandendo dunque le possibilità di accesso a questa tecnica per fini di diagnosi.
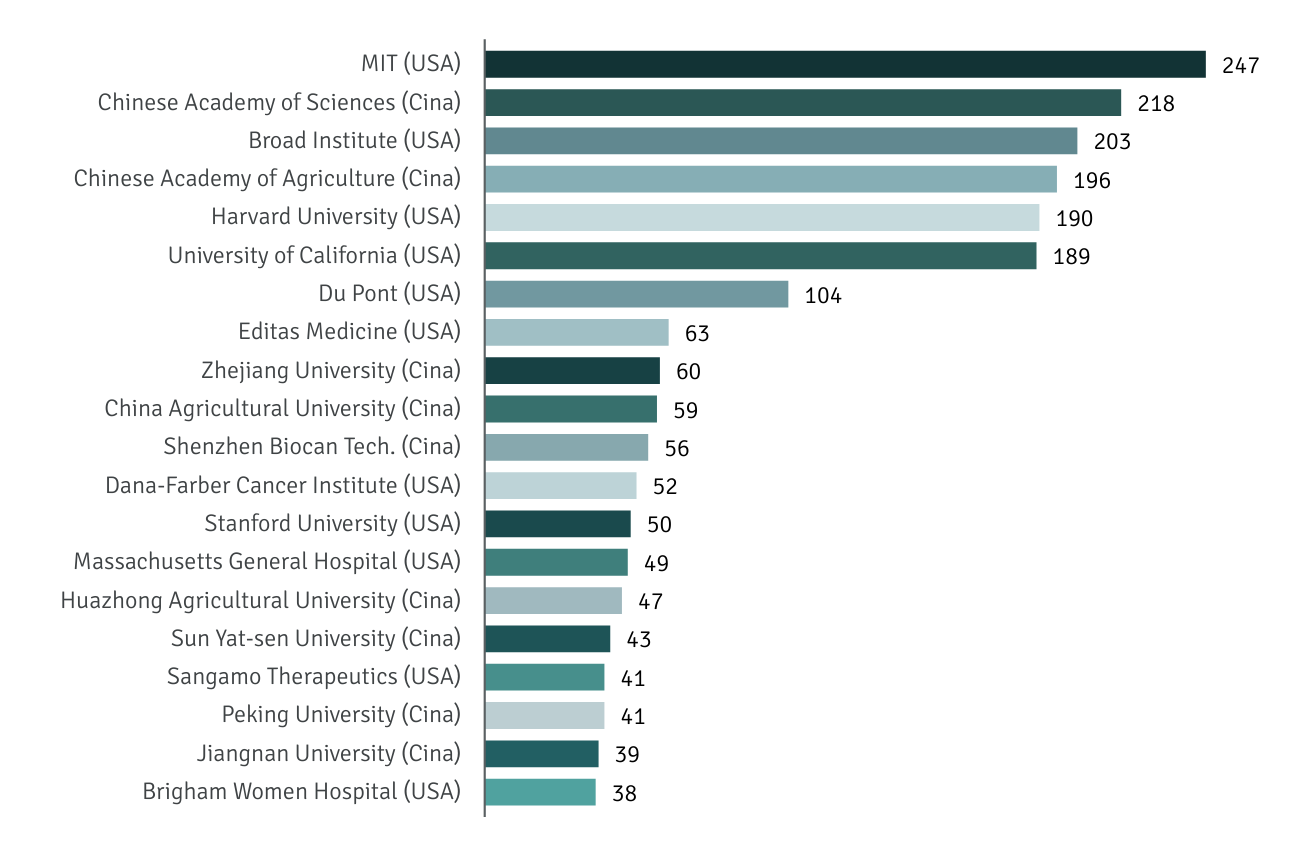
Le prime venti organizzazioni per numero di brevetti CRISPR. La competizione per i brevetti CRISPR-Cas9 ha dato origine a una contesa legale tra due istituzioni, il Broad Institute (istituto di genetica costituito congiuntamente da Harvard e MIT) e l’Università della California, Berkeley. È in questo ateneo che Jennifer Doudna ed Emmanuelle Charpentier hanno scoperto e perfezionato le funzioni di editing genetico di CRISPR. Fonte: IPStudies, CRISPR patent analytics, aggiornato ad agosto 2020.
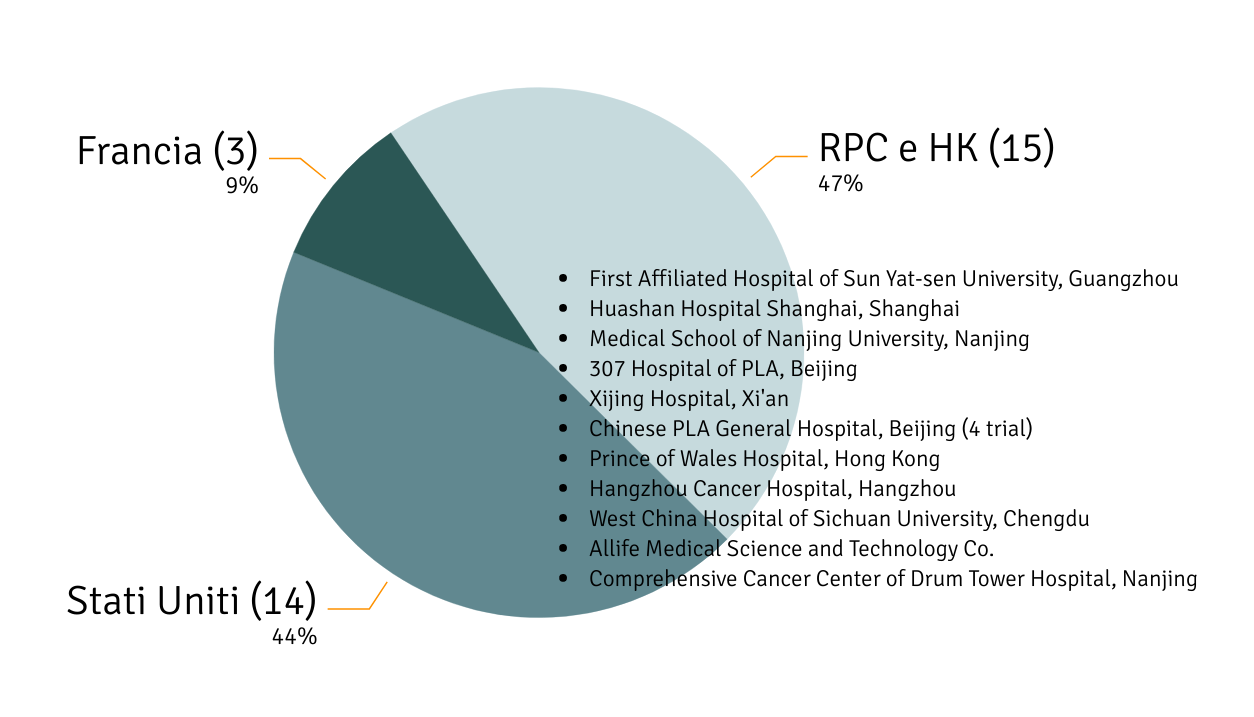
Trial clinici basati sulla tecnologia CRISPR. Il maggior numero di trial clinici in corso per la sperimentazione terapeutica di CRISPR avviene in Greater China. Tra gli ambiti testati vi sono cure per l’HIV, infezioni polmonari, neoplasie e leucemia. Fonte: ClinicalTrial.gov, U.S. National Library of Medicine, aggiornato ad agosto 2020.
La nascita di un dibattito interno
Dati gli investimenti e interessi in gioco non è sorprendente che alcuni attori si siano spinti al limite di ciò che è considerato eticamente praticabile, come gli esperimenti del 2015, 2017 e 2018 dimostrano. È bene, tuttavia, rimarcare che anche in Cina le risposte all’esperimento di He Jiankui furono univocamente negative sia da parte della comunità scientifica nazionale sia dei vertici del Partito-Stato. L’episodio del 2018 ha di fatto fornito uno stimolo per una normazione più chiara, articolata e severa della sperimentazione genetica. Pechino, allineandosi alle prassi internazionali, sembra dunque voler adottare un approccio precauzionale. L’impiego di CRISPR sul genoma umano è, infatti, considerato ancora poco sicuro. L’incertezza principale è tuttora rappresentata dalle “mutazioni fuori bersaglio”, ovvero mutazioni genetiche non volute che si attivano in segmenti di DNA diversi da quelli programmati con CRISPR. Rispetto a tecniche già affermate (come TALENs), CRISPR è in grado di intervenire su un numero più alto di geni in un unico intervento; il problema delle mutazioni fuori bersaglio pone dunque un rischio maggiore. Inoltre, i biologi sono ancora lontani da una conoscenza completa di tutte le funzioni del DNA e delle relazioni tra cellule; non si ha, dunque, una contezza precisa delle reazioni provocate dalla manipolazione del genoma.
Sono proprio queste grandi incertezze ad aver spinto la comunità scientifica a interrogarsi sull’utilizzo etico e le conseguenze sociali di CRISPR. Appena un mese prima della pubblicazione dell’articolo del team di Huang, nel marzo del 2015, i più importanti biologi molecolari, tra cui i pionieri di CRISPR-Cas9, si riunirono a Napa Valley per discutere dei vincoli etici che questa tecnologia avrebbe richiesto. Il risultato del forum fu una dichiarazione collettiva, pubblicata su Science, che scoraggia fortemente qualsiasi tentativo di alterazione della linea germinale umana per scopi clinici e di ricerca, auspicando inoltre l’apertura di un dibattito tra enti scientifici e organizzazioni governative per riflettere sulle implicazioni sociali, ambientali ed etiche di CRISPR. Un documento analogo, ma più esplicito nel condannare la sperimentazione sulla linea germinale, fu pubblicato su Nature da un altro gruppo di scienziati nello stesso mese. Entrambe le dichiarazioni non sono distanti dai principi e dai limiti già esposti nella “Convenzione sui diritti umani e la biomedicina” firmata a Oviedo nel 1997.
In Cina, una prassi di verifica e revisione etica della sperimentazione genetica esiste ed è normata dalla NHC, incaricata di stabilire le linee guida per la ricerca biomedica sugli esseri umani. Il primo tassello di questa regolamentazione fu posto nel 1993 tramite le “Misure amministrative per la sicurezza dell’ingegneria genetica” rilasciate dal MOST (il Ministero per la Scienza e la Tecnologia cinese). Queste disposizioni coprono ambiti molto ampi e non fanno menzione della sperimentazione sulla linea germinale umana. Nel 1998, vennero rilasciate le “Misure ad interim per la gestione delle risorse genetiche umane” mentre nel 2001 l’allora Ministero della sanità (oggi NHC) approvò le “Misure amministrative per le tecnologie di procreazione umana assistita”. Queste ultime “Misure” proibiscono le pratiche di fecondazione in vitro per la maternità surrogata, interdicendo la manipolazione genetica di gameti, zigoti ed embrioni umani a fini riproduttivi. Imponendo i medesimi principi nel campo della ricerca, le “Linee guida etiche per la ricerca sulle cellule staminali embrionali umane” del 2003 vietano la clonazione e alterazione degli embrioni umani a scopo riproduttivo, stabilendo inoltre che la coltivazione degli embrioni in vitro non può superare i 14 giorni dopo la fecondazione, in linea con gli standard internazionali. Nel 2016 vengono rilasciate le “Misure di revisione etica per la ricerca biomedica che coinvolge gli esseri umani” che dispongono la creazione di comitati etici indipendenti all’interno delle istituzioni coinvolte nella ricerca biomedica.
Il 2019 si rivela un anno fecondo per la regolamentazione del settore, com’era ipotizzabile a seguito del dibattito provocato dalla vicenda di He Jiankui. A marzo, il MOST rilascia una draft delle “Misure amministrative di sicurezza per la ricerca e lo sviluppo nelle biotecnologie”; a luglio, entrano in vigore i “Regolamenti per la gestione delle risorse genetiche umane” che aggiornano le “Misure ad interim” del 1998; a ottobre, viene rilasciata la prima bozza della Legge sulla biosicurezza, la cui seconda versione è stata presentata all’Assemblea nazionale del popolo nell’aprile 2020 e che include anche la creazione di un sistema efficiente di monitoraggio e risposta per il controllo delle epidemie. Questa prolifica normazione, tuttavia, non corrisponde ancora a un sistema di governance coeso e organico. La NHC non può, infatti, regolare le attività nelle università, ma solo negli ospedali e in altre istituzioni mediche. Inoltre, è ormai comprovata la diffusa inosservanza del divieto delle pratiche di maternità surrogata. Uno studio del 2014 stima che vi siano state in Cina almeno 25 mila nascite surrogate facilitate da 500 agenzie di riproduzione assistita non autorizzate.[14] Nel mondo accademico la supervisione non è sempre efficace e le procedure di consenso informato per chi si sottopone alle sperimentazioni, e di autorizzazione da parte dei comitati etici, sono spesso implementate velocemente e con gravi vizi di forma, come il caso di He Jiankui ha evidenziato. Ancora, come spesso accade nella frammentata legislazione cinese, non sono chiare le responsabilità legali in caso di inosservanza delle linee guida.
Nel luglio 2019, la Nona riunione del Gruppo guida per l’approfondimento complessivo delle riforme, guidata da Xi Jinping, ha approvato la creazione di un Comitato etico nazionale per la scienza e la tecnologia. Esso dovrà costituire un sistema di governance etica che sia comprensivo, standardizzato, coerente, che chiarisca le responsabilità legali e identifichi possibili faglie nella legislazione. Secondo un report della rivista Nature, alcuni biologi di punta, come il pioniere della bioetica in Cina Qiu Renzong, hanno inoltre proposto al Partito la creazione di un comitato composto da scienziati, fisici, filosofi, giuristi ed esperti di etica, per contribuire alla regolamentazione delle nuove tecnologie, incluse quelle digitali. L’incidente di He Jiankui ha, dunque, posto sotto i riflettori l’esigenza di una normazione della sperimentazione genetica più organica e trasparente, stimolando un dibattito in seno alla comunità scientifica cinese e tra i decisori. Nondimeno, occorre sottolineare che il rilievo internazionale dell’episodio ha determinato un danno in termini di immagine tale da erodere una quota significativa del soft power scientifico di Pechino. È dunque comprensibile che i vertici del Partito-Stato abbiano reagito rapidamente e stiano ora imbastendo i primi pilastri di uno spazio che, anche per le enormi potenzialità di attrazione di capitali, non può che essere normato e trasparente e possa rassicurare la comunità internazionale dell’impatto benefico della ricerca scientifica in Cina.

Avvenimenti salienti nella scoperta e nell’impiego di CRISPR. Nonostante la scoperta di CRISPR-Cas9 sia avvenuta negli Stati Uniti, la Cina ha raggiunto rapidamente lo stato dell’arte in diversi ambiti di applicazione.
Considerazioni conclusive
Le frizioni tecnologiche tra Cina e Occidente, in incubazione già da tempo ma slatentizzate negli ultimi anni, rischiano di oscurare alcuni aspetti più articolati e meno sensazionalistici del dibattito, ovvero le fratture che si stanno aprendo nel mondo della scienza, specialmente nelle biotecnologie, riguardo ai vincoli etici. Certamente, preoccupazioni di natura etica animano già il dibattito sull’automazione, sui big data, sulla privacy, sulle tecnologie per la sorveglianza e i sistemi di regolazione sociale come il social credit system. La sperimentazione genetica, tuttavia, pone la riflessione etica su un piano meno esposto al discorso pubblico. Ciò che è permesso e ciò che è interdetto sembrano avere un impatto meno immediato su dinamiche sociali direttamente percepibili. L’eterogeneità degli approcci regolativi si inscrive nelle diverse sensibilità che paesi differenti portano con sé e che sono informate da aspetti profondamente legati alla cultura, alla visione del mondo, a volte alla tradizione religiosa. Senza dubbio, anche le considerazioni legate alla competitività economica e alla sicurezza nazionale hanno un peso ragguardevole in questo dibattito.
Ciò che è però interessante rilevare è come l’accelerazione della Cina nell’ingegneria genetica non ponga solamente il problema di uno scontro tra approcci diversi alla ricerca scientifica. La velocità con cui le sperimentazioni cinesi hanno infranto alcuni tabù ha avuto la capacità di scomporre la già precaria unità di regole etiche condivise all’interno della comunità scientifica internazionale, alterando il sistema di incentivi, creandone di nuovi, e alzando la posta in gioco. Ad esempio, mentre Nature e Science, le più rinomate riviste scientifiche al mondo, rifiutarono di pubblicare l’esperimento di Huang nel 2015, non passò molto tempo prima che fosse un’altra rivista, Protein & Cell, a pubblicare la ricerca. I risultati dell’esperimento sono oggi ben integrati dentro il corpus di conoscenze che la comunità scientifica ha a disposizione. Tale fenomeno non è che un prodromo di ciò che è in gioco con altre tecnologie come il 5G, l’intelligenza artificiale e il riconoscimento facciale, per citarne solo alcune. Pechino sembra aver dimostrato in più occasioni di avere la capacità di aprire faglie che difficilmente possono essere ricomposte, ma che al contrario impongono un riassestamento delle prassi internazionali su un equilibrio differente.
La Cina, dal canto suo, si trova ancora una volta di fronte a un paradosso. Da una parte, Pechino ha bisogno di affermarsi come interlocutore credibile all’interno della comunità scientifica internazionale (lo dimostra l’attenzione per il proprio posizionamento nelle pubblicazioni scientifiche, nei ranking universitari e nei brevetti). Dall’altra, è proprio la Cina a sfidare alcune prassi condivise imponendo una nuova velocità su temi come la sperimentazione sulla linea germinale umana. Incalzati da questa rapidità, i paesi occidentali si troveranno a inseguire un difficile equilibrio tra due esigenze contrapposte: mantenere il passo e cercare di coinvolgere la Cina all’interno di una dialettica, per quanto possibile, condivisa.
[1] Davies Kevin, Barrangou Rodolphe, “COVID-19 and the CRISPR Community Response”, The CRISPR Journal 3 (2020) 2: 66-67.
[2] Acronimo di Clustered regularly interspaced short palindromic repeat-CRISPR associated protein 9
[3] Nella sperimentazione biomedica è ormai accettata, entro certi limiti, l’alterazione genetica delle cellule somatiche mentre è estremamente controversa la sperimentazione sulle cellule germinali (ovvero spermatozoi e ovociti). Essendo quest’ultime portatrici di caratteri ereditari, le modifiche indotte sono trasmissibili alle generazioni successive. Le cautele di scienziati, decisori ed esperti in vari campi derivano, oltre che dall’ereditarietà dell’alterazione genetica, anche da preoccupazioni di carattere sociale ed etico. L’affermarsi di questa pratica a scopi diversi da quelli clinici e terapeutici potrebbe favorire il riaffermarsi di pratiche eugenetiche. Ad oggi, la modifica della linea germinale umana è proibita per legge in circa 30 paesi.
[4] Tutti i dettagli di questa vicenda, compreso lo stato di salute dei tre bambini, sono stati secretati dalla Corte del distretto di Nanshan, Shenzhen, per proteggere la privacy delle persone coinvolte.
[5] Anche le basi scientifiche e i risultati dell’esperimento di He sono stati duramente contestati a causa della metodologia debole e opaca.
[6] La Higher Education Press, il Beijing Institute of Life Science, la Chinese Academy of Sciences e la Biophysical Society of China.
[7] Per una descrizione più esaustiva di CRISPR-Cas9 si rimanda all’introduzione della U.S. National Library of Medicine, accessibile online all’indirizzo https://ghr.nlm.nih.gov/primer/genomicresearch/genomeediting
[8] ClinicalTrials.gov è un database voluto dall’U.S. Department of Health and Human Services nel 2000 che rappresenta attualmente il più vasto database di trial clinici, finanziati da fondi pubblici e privati, al mondo.
[9] Martin-Laffon Jacqueline, Marcel Kuntz, and Agnès E. Ricroch, “Worldwide CRISPR patent landscape shows strong geographical biases”, Nature Biotechnology 37 (2019): 601-621.
[10] Xu Lei, Jun Wang, Yulin Liu, Liangfu Xie, Bin Su, Danlei Mou, Longteng Wang et al., “CRISPR-edited stem cells in a patient with HIV and acute lymphocytic leukemia”, New England Journal of Medicine 381 (2019) 13: 1240-1247.
[11] Paul Joseph e Yiping Qi, “CRISPR/Cas9 for plant genome editing: accomplishments, problems and prospects”, Plant cell reports 35 (2016) 7: 1417-1427.
[12] Tom Hancock, Wang Xueqiao, Emiko Terazono, Andres Schipani, “Europe and Brazil help fill China’s 10m-tonne pork shortfall”, Financial Times, 10 settembre 2019, disponibile all’Url https://www.ft.com/content/ccf12bba-d2d4-11e9-8367-807ebd53ab77
[13] National Human Genome Research Institute, accessibile online all’indirizzo: https://www.genome.gov/about-genomics/fact-sheets/DNA-Sequencing-Costs-Data
[14] Qiao Jie e Huai L. Feng, “Assisted reproductive technology in China: compliance and non-compliance”, Translational pediatrics 3 (2014) 2: 91.
“The conference is the outcome of one year of meetings within the New Technologies for Peace working group. During our gatherings, scholars, diplomats, experts... Read More


Corso Valdocco 2, 10122 Torino, Italy
Sede legale: Galleria S. Federico 16, 10121 Torino
Copyright © 2026. Torino World Affairs Institute All rights reserved
